
【編集部より】
本記事は特定の製品・クリニック・業者を
断罪するものではありません。
日本の美容医療市場における
承認・流通の構造的問題を、
消費者と医療従事者の双方に向けて
提示することを目的としています。
あなたが受けた、あるいは受けようとしているその施術。
体に入れる前に、知っておくべきことがあるかもしれません。
「承認済み」という言葉の中身を、
確認したことがあるか。
前編では、「マーケティング先行」という
美容医療業界の構造を解剖した。
しかし、問題はそれだけではない。
「承認済み」という言葉そのものが、
実は機能していないケースが存在する——。
INDEX
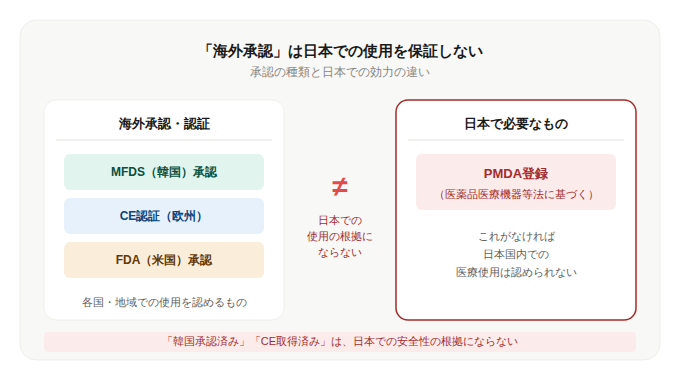
「海外承認」は日本での使用を保証しない
美容医療の現場では、
製品や機器の安全性の根拠として
以下のような承認・認証が頻繁に引用される。
・MFDS(韓国食品医薬品安全処)承認
・CE認証(欧州)
・FDA(米国)承認
消費者にとっても医師にとっても、
これらは「お墨付き」の代名詞だ。
「海外で認められた=安全」という文脈で、
疑いなく使われている。
しかし、日本国内で医療行為に用いる製品・機器は、
原則として日本の公的機関(PMDA)への
承認・登録が必要だ。
海外機関の承認は、
日本での使用の正当性を保証しない。
これは解釈の問題ではなく、制度の問題だ。
「調べても出てこない」——承認の実態
ここからが、より深刻な問題だ。
「承認を取得済み」と謳いながら、
日本の公的データベースを
どれだけ丹念に調べても——
登録が、見当たらない。
承認番号を直接問い合わせなければ確認すらできない。
公式広報では「承認済み」と発信されている。
しかしデータベース上に、その名前は存在しない。
AIツールを使い、あらゆる角度から調べても——
結果は同じだ。
「同じ承認基準をクリアしているなら、
当然登録されるはずでは?」その疑問に、現状の仕組みは答えを与えてくれない。
なぜ登録されているものとされていないものが
混在しているのか。
誰も、明確には説明できないのだ。
「承認済み」という言葉は、
中身が検証されなければ意味をなさない。
消費者保護の機能を、果たしていない。
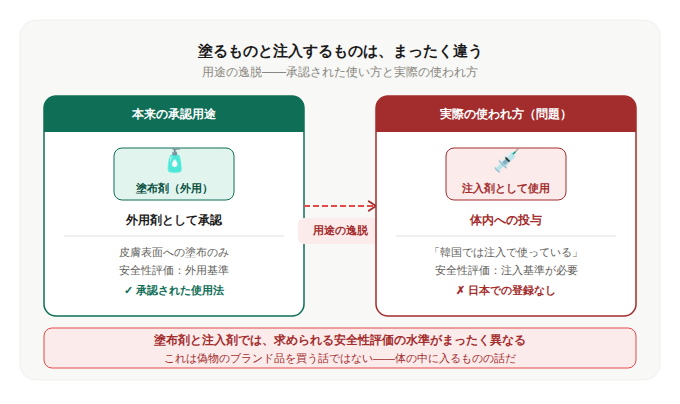
より深刻な問題——塗るものと注入するものは、違う
NEROが特に注視しているのが、
「用途の逸脱」という問題だ。
塗布剤(外用剤)として承認・流通している製品が、
日本市場では注入剤として
紹介・販売・使用されているケースもあるという。
「韓国では何年も前から注入で使っている」
「欧州でも5年前から当たり前」——
そう発信する声がある。
海外の医師インフルエンサーがこうした発言をし、
日本のクリニックや広告媒体が
精査せずに拡散する。
しかし蓋を開ければ、
日本での注入剤としての登録が存在しない。塗布剤と注入剤では、
求められる安全性評価の水準がまったく異なる。
体表面に塗るものと、体内に直接投与するものを、
同じ基準で語ってはならない。
これは、偽物のブランド品を買ってしまう話ではない。
体の中に入るものの話だ。
誰がこの構造を支えているか——無責任の連鎖
こうした事態が起きる背景には、
複数のプレイヤーにまたがる連鎖がある。
並行輸入業者が、正規品として製品を持ち込む。
代理店が、承認状況を精査せずに展開する。
広告媒体が、そのまま掲載する。
業界イベントやセミナーの場でさえ、
販売代理店が登壇し、
医師たちに向けてプレゼンが行われている。
医師が、「海外では使われている」という
情報だけで採用を決める。
消費者が、SNSのビフォーアフターを見て
施術を受ける。
誰一人として「待て」と言う者がいない。
倫理よりビジネスが優先され、
精査されないまま情報が拡散し、
消費者はそれを「信頼できる情報」として受け取る。この連鎖の末端にいるのは、常に患者だ。
消費者が今日からできること
この構造の中で自分を守るために、
施術前に最低限確認すべき問いを3つ提示する。

① PMDAへの登録確認
「韓国承認」「CE認証」ではなく——
「日本の公的機関への登録番号を
教えてもらえますか?」と聞くこと。
答えに詰まるクリニックとは、距離を置くべきかもしれません。
② 用途の確認
「これは注入剤として承認されていますか?
塗布剤ではありませんか?」「海外では注入で使われている」は、
日本での注入の根拠にならない。
用途の範囲外での使用は、リスクを伴う。
③ 副作用対処の確認
承認が不明確な製品は、
副作用への対処法も確立されていないことがある。「副作用が出た場合、どう対処しますか?」
この一問を、施術前に必ず投げかけること。
医療従事者へ——「仕入れる前に調べる」は医療倫理の基本だ
新しい製品・機器を導入する際、
クリニック側には最低限の確認義務がある。
日本の公的機関への登録確認。
承認された用途の範囲確認。
並行輸入品でないかの確認。
「メーカーが承認済みと言っていた」は、
患者への説明責任を果たしたことにはならない。情報の一次確認を代理店やメーカーに委ねることは、
医療従事者としての判断の放棄だ。
「この製品は本当に、
患者の体内に入れていいものか」——
その問いを、導入の前に
必ず自分自身に課すこと。
まとめ
- 「海外承認済み」は日本での使用の正当性を保証しない
- 承認を謳いながら日本の公的データベースに登録が確認できない製品が流通しているケースがある
- 塗布剤として承認された製品が注入剤として使用されているケースがある
- この構造は代理店・媒体・医師・消費者にまたがる「無責任の連鎖」によって成立している
- 消費者は「PMDA登録」「用途の確認」「副作用対処の明確化」という3点を施術前に確認すること
✦ NEROが真っ直ぐに向き合う「メディアの使命」
美容医療は消費財ではなく、医療だ。
私たちNEROは、業界の耳に痛い構造的問題にも
真っ直ぐに向き合い、
フラットな情報を提供することで、
読者とクリニックの間に
真の信頼関係を築くための架け橋でありたいと考えている。
特定の誰かを批判するのではなく、
業界全体をより良くしていくための「問い」を立て続けること。
「これは本当に安全か」——
その問いを、業界の誰かが声に出し続けなければならない。
その役割を、NEROは引き受ける。
※本記事における承認状況に関する情報は、取材・調査時点での内容に基づくものです。承認状況は変動する可能性があり、最新情報は各公的機関の公式データベースにてご確認ください。







