
📌 記事をざっくりまとめると…
・中国が美容ヒアルロン酸フィラー審査ガイドライン(2026)を改訂
・臨床試験・安全性・製品特性データの提出要件を強化
・急成長する美容医療市場で医療機器審査の科学的要求が明確化
中国の医療機器審査機関
CMDE(国家薬品監督管理局 NMPA 医療機器評価センター) は2026年2月、
「美容用ヒアルロン酸ナトリウム注入剤登録審査ガイドライン(2026年改訂版)」
を公表した。
対象となるのは、
・ほうれい線修正
・しわ改善
・顔面ボリューム形成
などに使用される
美容用ヒアルロン酸フィラー製品である。
改訂ガイドラインは
公布と同時に施行された。
今回の改訂では
・製品特性に基づく科学的データ提出
・臨床性能評価
・生体内分解試験
などが体系化され、
美容フィラーに対する
医療機器審査の基準がより明確化された。
中国のフィラー審査、何が変わったのか
改訂ガイドラインの特徴は
「研究項目マトリックス」の導入である。
ガイドラインでは
30以上の性能評価項目が提示され、
原則として
各項目の研究データ提出が求められる。
企業が
「該当しない」と判断する場合でも、
科学的根拠による説明が必要となる。
これにより
・審査の透明性
・科学的裏付け
が強化された。
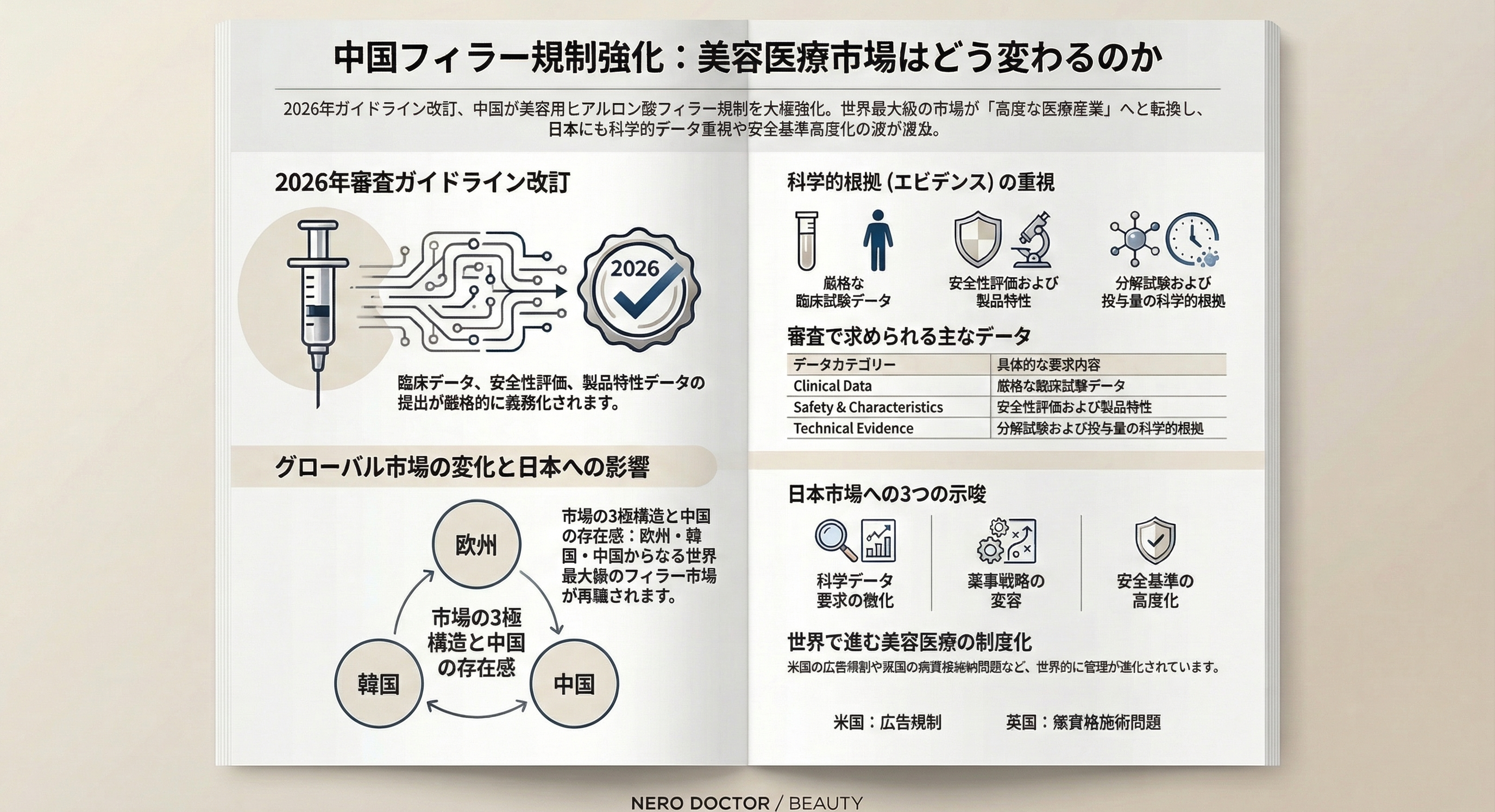
フィラー審査はここまで厳格化
強化された主な評価ポイント
今回の改訂では、
以下の分野で要求が明確化された。
■ 原材料の特性評価
架橋前ヒアルロン酸について
・分子量
・分子量分布
などのデータ提出が求められる。
■ 分解・代謝試験
製品ごとの
in vivo分解試験
など、体内挙動を示すデータが必要となる。
■ 投与量の科学的根拠
以下の項目について
臨床または動物試験データによる裏付けが必要となる。
・最大単回投与量
・1回施術の最大投与量
・再注入間隔
■ 生物学的安全性評価
従来の生体適合性評価に加え、
・粒子関連リスク
・最大投与量シミュレーション
など、
リスク評価範囲
が拡大された。
なぜこのニュースが業界で注目されるのか
美容医療市場への影響
中国は現在、
世界最大級の美容医療市場の一つであり、
ヒアルロン酸フィラー市場も
急速に拡大している。
今回の改訂により
・臨床試験設計
・製品データ管理
・薬事申請戦略
など、
製品開発段階からの規制対応
がより重要になる可能性がある。
特に海外メーカーにとっては
中国市場への製品登録戦略
にも影響する可能性がある。
編集長POINT|美容医療市場の拡大と規制の精緻化
ヒアルロン酸フィラーは、
美容医療では比較的広く普及した施術である。
一方で各国では
美容医療で使用される製品に対する
医療機器としての科学的審査要求
が徐々に強化されている。
今回の中国ガイドライン改訂は
原材料特性
臨床データ
安全性評価
など、
製品ごとの科学的裏付け
をより明確に求める内容となった。
美容医療市場の拡大に伴い、
製品審査の枠組みも
よりデータ重視の方向へ
と進んでいる。
まとめ
・中国が美容ヒアルロン酸フィラー審査ガイドラインを改訂
・臨床性能・製品特性・安全性データ提出を体系化
・30以上の性能評価項目を提示
・美容フィラーに対する医療機器審査基準が明確化
出典:中国 国家薬品監督管理局(NMPA) 医療機器評価センター(CMDE)
「美容用ヒアルロン酸ナトリウム注入剤登録審査ガイドライン(2026年改訂版)の公布に関する公告(2026年公告第5号)」






