
📌 記事をざっくりまとめると…
- マレーシアが美容医療デバイスを医療機器規制対象に
- レーザー、HIFU、脂肪吸引機器などが対象
- 急拡大する美容医療市場への安全規制強化
マレーシア医療機器当局(Medical Device Authority:MDA)は2026年2月、
美容医療で使用される特定の機器を医療機器規制の対象とする新制度を公布した。
新制度「Medical Device (Designated Medical Devices) Order 2026」は、
美容医療分野で使用される技術を正式に医療機器規制フレームワークへ組み込むものである。
施行は2026年6月1日を予定しており、
-
製品登録
-
安全評価
-
使用者資格
などの要件が求められる。
急速に拡大するアジアの美容医療市場に対する、
安全規制強化の典型例といえる。
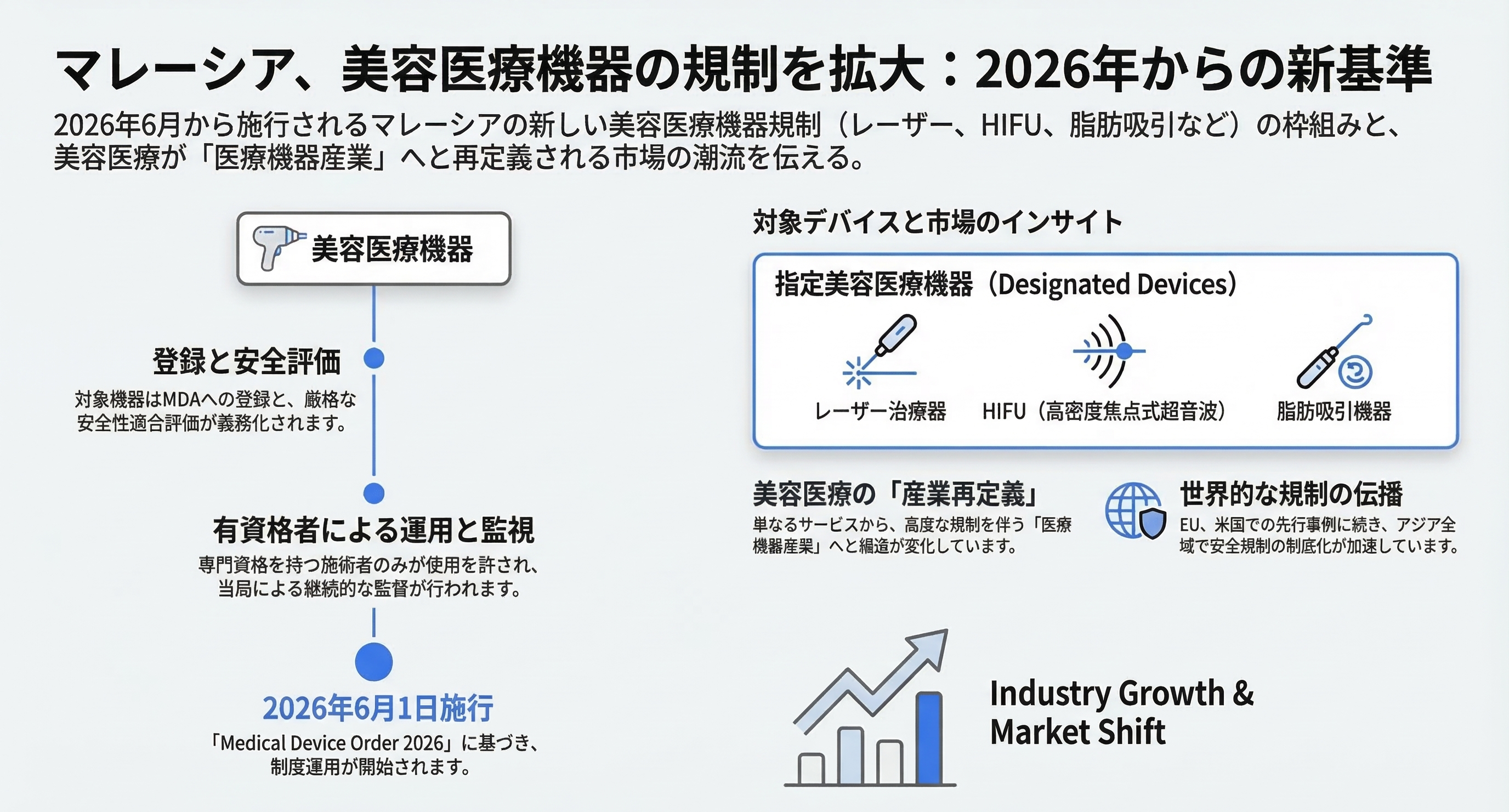
マレーシアで何が変わるのか
マレーシア医療機器当局(MDA)は2026年2月、
美容医療で使用される機器を対象とする新制度
を公布した。
この制度により、
これまで規制が曖昧だった一部の美容医療機器が
正式な医療機器管理制度の対象となる。
施行日は2026年6月1日で、
対象機器には医療機器としての登録や適合評価が求められる可能性がある。

規制対象となる美容医療機器はどれか
今回の制度では、
美容医療で広く使用されている次の機器が対象に含まれる。
-
レーザー治療機器
-
HIFU(高密度焦点式超音波)
-
脂肪吸引機器
-
その他の美容医療関連デバイス
これらの機器は今後、
医療機器としての登録
安全性評価
規制審査
などの対象となる可能性がある。
なぜ今、美容医療デバイス規制なのか
背景にあるのは、
アジア地域で急拡大している美容医療市場である。
レーザー治療
HIFU
医療痩身
など、
医療機器を使用する美容施術が増加している。
その結果、
機器の安全性
使用者資格
医療責任
を制度的に管理する必要性が高まっている。
今回の制度は、
美容医療機器の安全管理を制度化する動きと位置づけられる。
メーカー・クリニックに求められる対応
新制度の導入により、
美容医療機器メーカーや販売企業には
医療機器登録の確認
技術文書の整備
規制適合の確認
などの対応が求められる可能性がある。
また、
対象機器は
資格を持つ施術者による使用が前提
とされており、
美容医療施術の安全性向上を目的としている。
編集長POINT|美容医療は「医療機器産業」へ
美容医療市場は現在、
単なる美容サービスから
医療機器産業へと構造が変わりつつある。
レーザー
HIFU
RF治療
などの技術は、
高度な医療機器として
規制対象に組み込まれる流れが強まっている。
マレーシアの今回の制度は、
美容医療市場の拡大に合わせて
安全規制を制度化するアジアの動きを象徴するものといえる。
今後、
同様の規制強化は他のアジア諸国にも広がる可能性がある。
まとめ
-
マレーシアが美容医療デバイス規制を新制度で導入
-
レーザー・HIFU・脂肪吸引機器などが対象
-
2026年6月に制度施行予定
-
美容医療市場の拡大に伴う安全規制強化
出典:Medical Device Authority Malaysia
Cisema Regulatory Update






