
📌 記事をざっくりまとめると…
✔ iPS細胞を使った再生医療製品が世界で初めて薬事承認
✔ 心不全治療「リハート」とパーキンソン病治療「アムシェプリ」
✔ 日本の条件付き早期承認制度によって実用化が加速
✔ 実際の治療は2026年夏以降の見込み
✔ 再生医療は研究段階から臨床医療のフェーズへ
iPS細胞を用いた再生医療が、ついに実用化の段階へと踏み出した。
厚生労働省は2026年3月、
iPS細胞を用いた2つの再生医療製品を
世界で初めて薬事承認した。
対象は重症心不全とパーキンソン病
条件付き承認制度のもと、
早ければ2026年夏以降、
実際の治療として使用される見通しだ。
研究段階にとどまってきた再生医療は、
いま臨床医療へと移行する転換点を迎えている。
今回の承認は
単なる医療技術の進歩ではない。
再生医療という
新しい医療産業の始まりを示す出来事でもある。
INDEX
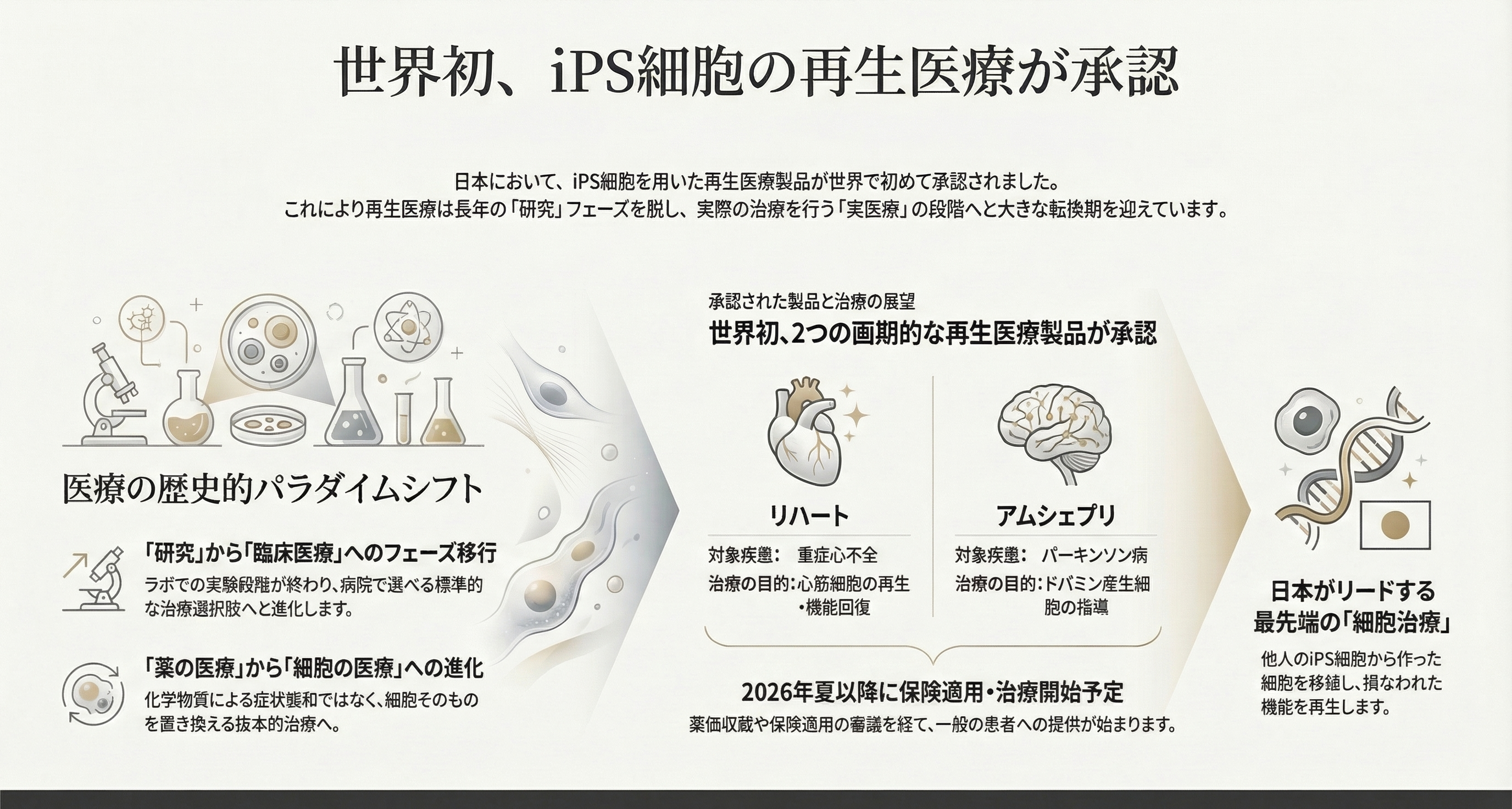
世界初、iPS細胞の再生医療が薬事承認
厚生労働省は2026年3月6日、
iPS細胞を用いた2つの再生医療製品を条件付きで製造販売承認したと発表した。
承認されたのは次の2製品。
重症心不全治療「リハート」
パーキンソン病治療「アムシェプリ」
iPS細胞を使った再生医療製品が薬事承認されるのは
世界で初めてとなる。
今後は中央社会保険医療協議会で保険適用の審議が行われ、
実際の治療で使用されるのは早くても2026年夏以降になる見通しだ。
厚生労働省の上野賢一郎厚生労働相は
「日本のみならず世界中の患者の皆様の救いとなることを願っている」
と述べている。
心不全とパーキンソン病への再生医療
今回承認された製品は
従来治療では改善が難しい重症患者を対象とする再生医療だ。
重症心不全治療「リハート」
大阪大学発ベンチャー
クオリプスが開発。
iPS細胞から作製した
心筋細胞シート
を心臓の表面に移植し、
心機能の回復を目指す。
重症心不全では
・薬物治療
・補助人工心臓
・心臓移植
などが選択肢となるが、
ドナー不足などの問題も多い。
再生医療は
新たな治療選択肢となる可能性がある。
パーキンソン病治療「アムシェプリ」
住友ファーマが申請した再生医療製品。
iPS細胞から作製した
神経前駆細胞
を脳に移植し、
神経細胞の機能回復を目指す。
パーキンソン病は
ドーパミン神経の減少
によって運動障害が進行する神経疾患で、
根治療法は確立されていない。
「条件付き承認制度」で実用化を加速
今回の承認は
条件・期限付き承認制度
によるものだ。
この制度では
・安全性が確認されている
・有効性が推定されている
段階で
早期に薬事承認が行われる。
その後
・リハート:75症例
・アムシェプリ:35症例
の臨床データを収集し、
7年以内に本承認を取得する必要がある。
再生医療は
研究から実用化まで長い時間がかかる。
この制度は
患者へ治療を早く届けるための日本独自の仕組みとして
世界から注目されている。
再生医療は「研究」から「臨床」へ
iPS細胞を用いた再生医療は現在
・脊髄損傷
・心不全
・1型糖尿病
・角膜疾患
などの分野で研究が進んでいる。
脊髄損傷の研究では
神経細胞移植により
患者が立てるまで回復した症例
も報告されている。
これまで再生医療は
研究段階にとどまることが多かった。
しかし今回の承認は
再生医療が実際の医療として動き始めた転換点
と見ることもできる。
急拡大する再生医療市場
再生医療は
医療産業としても急速な成長が予測されている。
市場調査によると
日本の再生医療市場は
2025年〜2030年で43億ドル以上の成長が見込まれ、
年平均成長率は
18.3%
と予測されている。
市場拡大の背景には
・高齢化社会
・慢性疾患の増加
・医療技術の進歩
がある。
さらに日本は
・再生医療安全確保法
・条件付き早期承認制度
・大学発バイオベンチャー
といった制度環境が整っており、
再生医療の先進国として世界から注目されている。
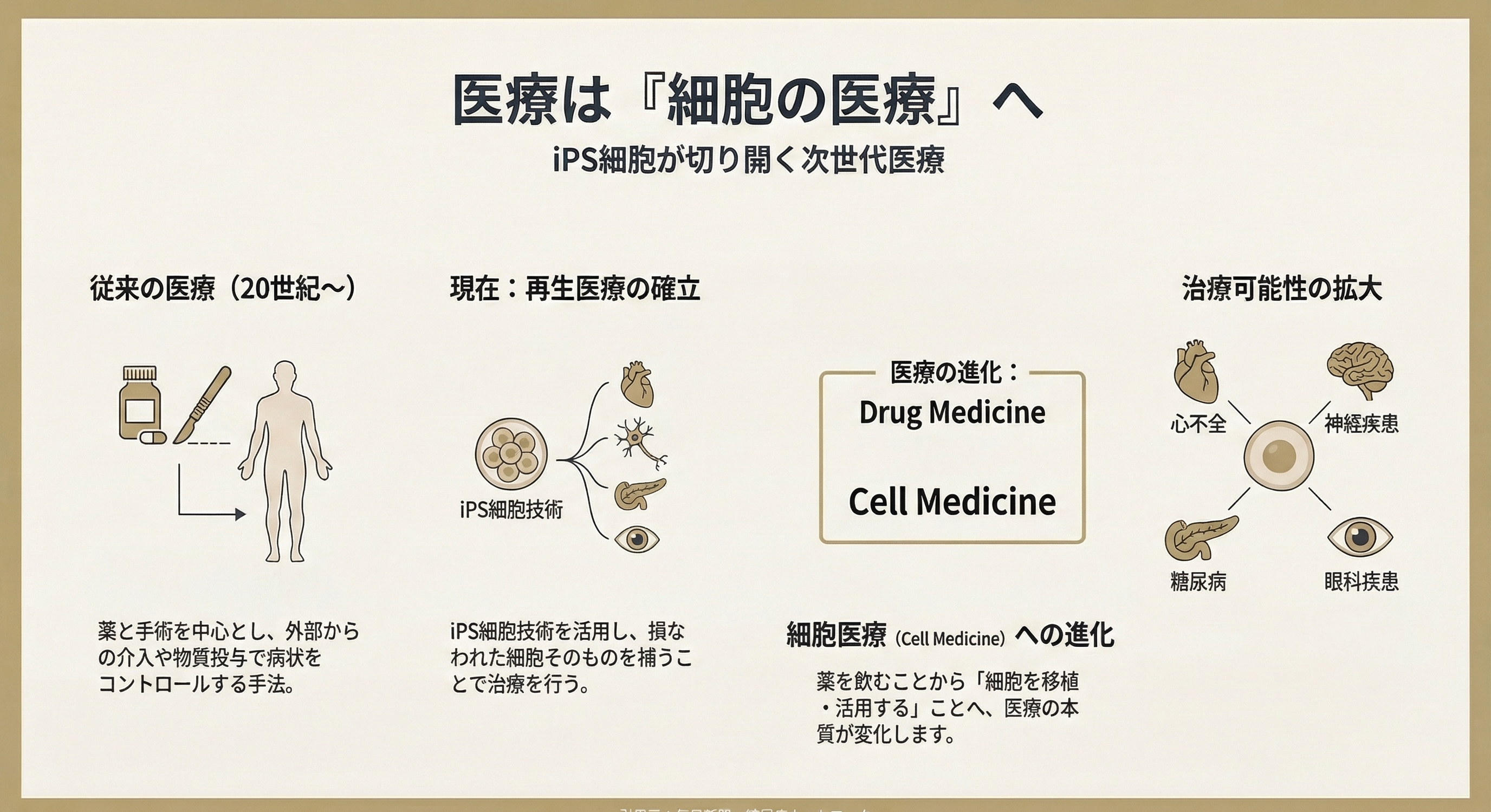
編集長POINT|「薬の医療」から「細胞の医療」へ
20世紀の医療は
薬と手術の医療
だった。
しかし再生医療が普及すれば
医療は
細胞そのものを治療として使う時代
へと移行する。
いわば
Drug Medicine → Cell Medicine
という転換だ。
今回の承認は
単なる新しい治療の誕生ではない。
医療そのものの構造が
変わり始めた瞬間なのかもしれない。
まとめ
✔ iPS細胞再生医療製品が世界で初めて薬事承認
✔ 心不全・パーキンソン病の新たな治療法
✔ 実際の治療は2026年夏以降の見込み
✔ 再生医療は研究段階から臨床医療へ
✔ 医療は「細胞の医療」へ移行する可能性







